
文章内容
1. 8-氧鸟嘌呤的配对方式
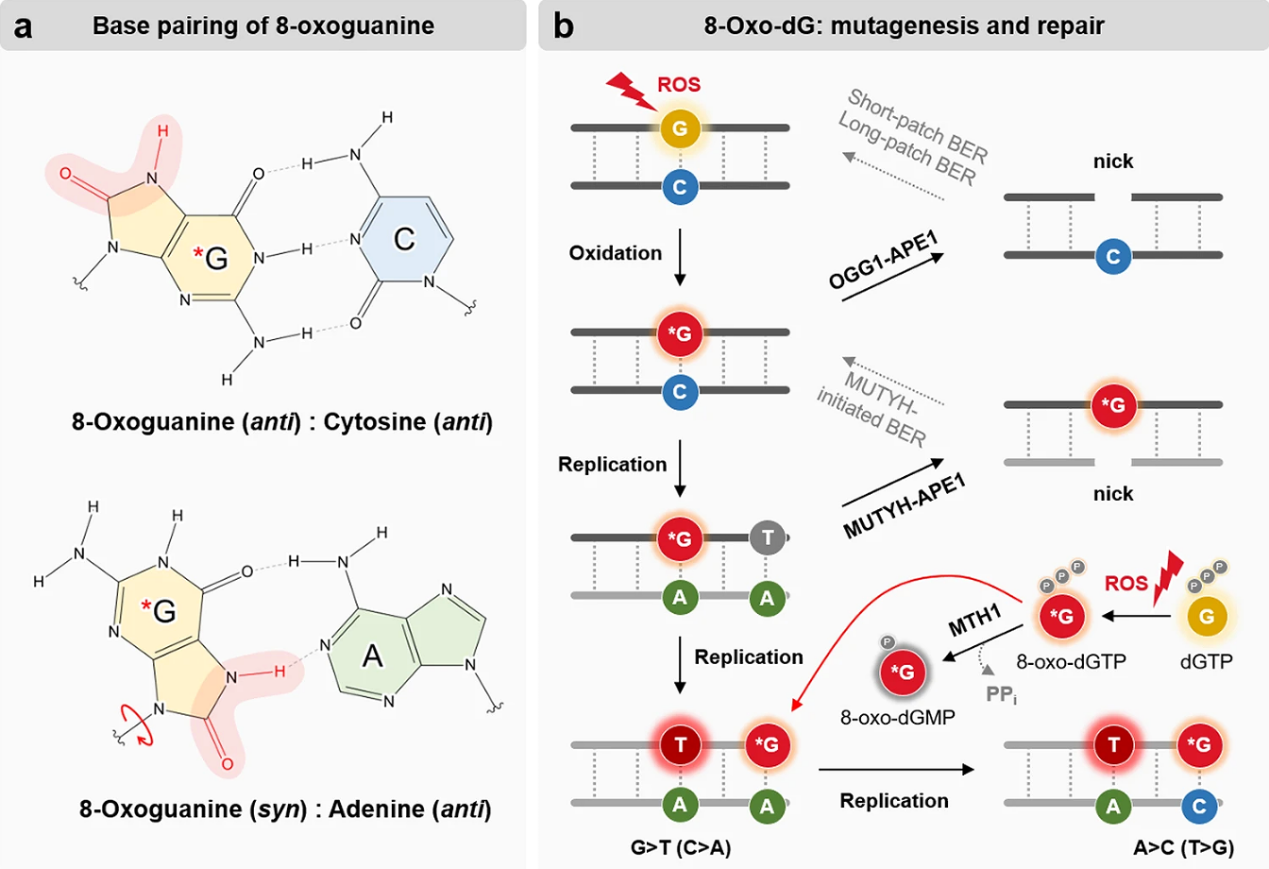
8-氧鸟嘌呤的关键特征是其顺势构象与腺嘌呤碱基对发生Hoogsteen碱基配对,而它的反式构象仍然作为一个未氧化的鸟嘌呤与胞嘧啶配对(图1a)。因此,8-oxo-dG导致鸟嘌呤向胸腺嘧啶转位,导致突变发生(G > T,与C>A相同)。为了防止这种损伤,8-氧鸟嘌呤DNA糖基化酶(OGG1)通过碱基切除修复(BER)途径识别、移除和修复8-oxo-dG10(图1b)。除了遗传信息的变化外,8-oxo-dG可以作为一种表观遗传标记,影响启动子中的调节元件、CpG岛的甲基化和分布。
2.DNA上发生的8-oxo-dG
8-oxo-dG具有高度的诱变性,它倾向于以syn顺式构象与腺嘌呤配对(图1a),在DNA复制过程中导致鸟嘌呤-胸腺嘧啶突变(G > T,与C>a相同),DNA聚合酶β(pol β)以syn构象容纳8- oxo-dG模板,从而将腺嘌呤合并到复制链中(图1b)。8-oxo-dG不*可以在DNA分子中形成,也可以在游离核苷酸中形成(图1b),这些游离核苷酸特别容易受到氧化损伤(8-oxo-dGTP)。由于8-oxo-dGTP引起pol β活性位点的变化,它的协同构象可以插入到相反的腺嘌呤中,避免被识别为受损,从而导致A>C的突变(与T>G相同),称为聚合酶诱导的细胞毒性(图1b)。
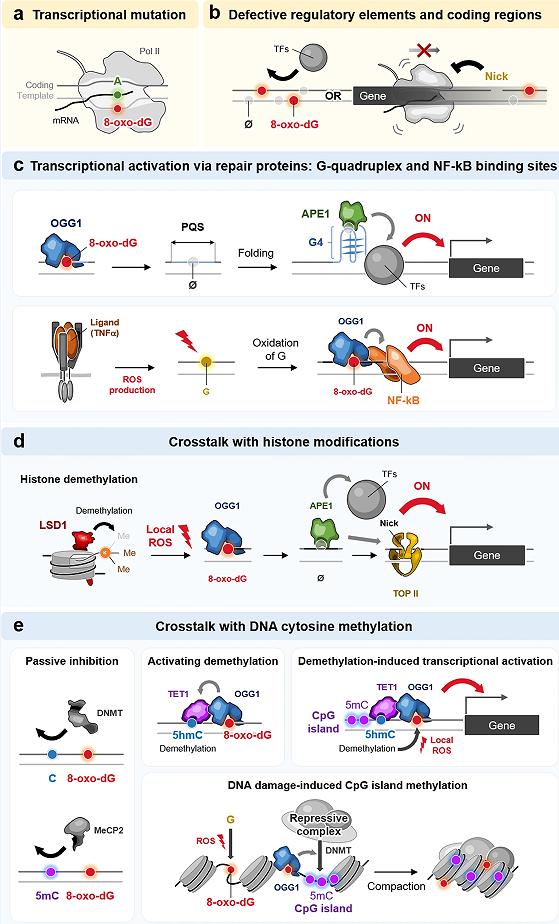
8-oxo-dG修饰不*能改变复制过程中的DNA信息(G > T转位),还能介导转录突变,调控遗传信息。尽管RNA聚合酶具有高保真度,但模板链中的8-oxo-dG可以直接转录,由于8-oxo-dG-A碱基配对,导致mRNA中的C > A转位,并且位于编码序列中的8-oxo-dG导致错误蛋白的翻译(图2a),这些蛋白经过不增殖的细胞而不进行DNA复制。8-oxo-dG及其修复中间体(如AP位点)可以通过影响转录元件的完整性来影响基因的表达(图2b),即使是位于编码基因非转录DNA链的,它也会通过转录中的调节元件抑制转录。
4. 8-氧鸟嘌呤转录调控的表观遗传作用
8-oxo-dG修饰不*损害DNA信息,而且作为一种表观遗传标记,与其修复中间体一起介导转录调控。除了G-四联体外,NF-kB转录因子的调控结合位点与8-oxo-dG与OGG1相互作用,促进转录**(图2c)。8-oxo-dG与组蛋白去甲基化相关,其中DNA氧化由去甲基化反应中产生的局部ROS诱导,随后与OGG1结合,介导转录调控(图2d),对于DNA胞嘧啶甲基化(5-甲基胞嘧啶,5mC),8-oxo-dG降低了与DNA甲基转移酶(DNMTs)的结合亲和力,从而抑制了CpG岛的甲基化(图2e),并且在氧化应激诱导的DNA去甲基化过程中,OGG1在识别8-oxo-dG损伤和招募TET1方面发挥了重要作用,TET1可以将邻近的5mC氧化为5-羟甲基胞嘧啶(5hmC)使DNA发生去甲基化(图2e)。
5. RNA中的8-氧鸟嘌呤
对8-oxo-dG的研究相比,对O8G的研究较少,其修复机制和调控功能尚不清楚。虽然DNA和RNA都能与ROS发生反应,但RNA的独特特性使其容易被氧化。RNA氧化可严重导致编码和非编码RNA的功能障碍和调节,这与氧化作用下的病理生理后果有关。因此,O8G不*参与氧化损伤,而且作为一种表转录修饰。
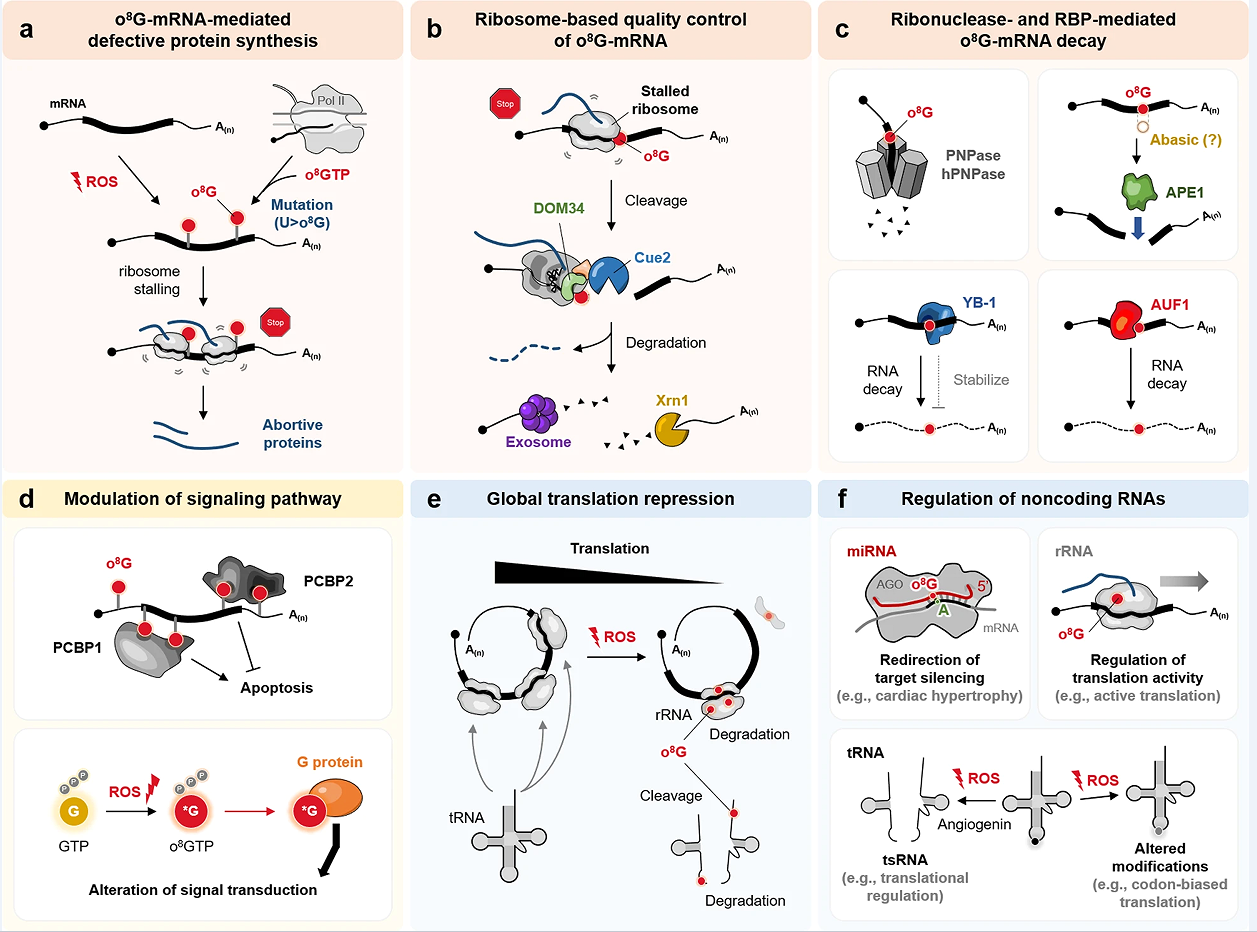
文章提出细胞质RNA的氧化修饰,可能包括mRNA、rRNA、tRNA和miRNA,均已被提出在氧化还原相关的疾病表型中发挥作用。mRNA中的O8G会恶化密码子-反密码子的相互作用,抑制翻译,并且会降低了遗传信息的质量,导致核糖体停滞,并通过改变碱基配对(O8G-A)合成受损的蛋白质。此外,mRNA中的O8G对其编码能力非常有害,因为它会导致核糖体停滞,随后产生流产蛋白(图3A),从而增加细胞毒性,恶化核糖体稳态,组织核糖体**no-go衰变(NGD)(图3b)。O8G能直接被核糖核酸降解酶(PNPase和APE1)和RBPs(YB-1和AUF1)识别,作为核糖体**的mRNA质量控制的一部分,但O8G可以作为一种表转录修饰,标记转录后基因抑制的选择性mRNA降解(图3c)。
6.信号通路的调节
PCBP1只通过其两个与RNA结合的KH结构域结合严重氧化的RNA,并不会使靶mRNA不稳定,而是**导致凋亡细胞死亡的信号通路(图3d)。在没有PCBP1的情况下,caspase-3**和PARP裂解减少。作者认为PCBP1与过量的O8Gs结合可启动一个损伤信号通路,导致氧化应激下的细胞凋亡。相反,即使PCBP2结合了严重氧化的O8G-RNA,PCBP2也抑制了ROS介导的细胞死亡(图3d)。此外,在氧化应激过程中,游离O8GTP浓度的增加可以调节小G蛋白的活性(图3d)。在一定条件下,O8G通过O8G-RNA或游离的O8GTP调节多种信号通路,诱导细胞凋亡,抑制炎症反应。目前,O8G在调节信号通路中的具体作用和机制也有待进一步研究。
7.翻译抑制
在H2O2处理后的大肠杆菌中,rRNA中的O8G**增加,而rRNA和tRNA的折叠结构在体外对其氧化没有保护作用。在AD患者的大脑中,核糖体功能障碍与作为早期事件的RNA氧化增加有关,导致蛋白质合成的速率和能力下降。表明如果翻译机制中产生O8G修饰,整体翻译水平立即下降(图3e)。此外,tRNA在氧化应激反应中经历特异性的切割,导致功能性tRNA池的下调,从而限制翻译延伸过程。考虑到细胞中大部分RNA由rRNA和tRNA组成,O8G修饰的总体方向是抑制整体翻译,其程度依赖于细胞的氧化还原状态(图3e)。
8.非编码RNA的调控
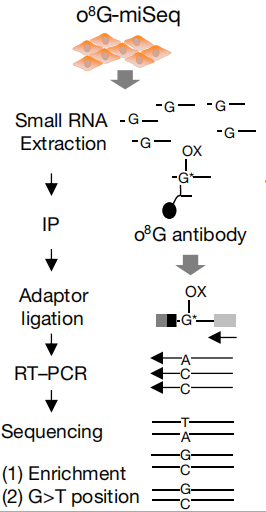
根据其靶点的功能,miRNA具有不同的病理生理作用。因此,种子序列的任何改变都可以改变不同的靶转录本组,导致miRNA介导的功能的重定向(图3f)。一般来说,核糖体的氧化抑制了它们的活性,但活性位点的特定位置的氧化促进了翻译(图3f),此外,氧化应激已被证明可以通过特定的酶(如人类中的血管生成素200,酵母中的Rny1)诱导tRNA裂解,从而赋予特定的调控和功能,而不**是作为氧化损伤的副产物(图3f)。同时,作者也表明通过开发O8G测序方法(o8 G- miSeq)可以精确鉴定了心脏miRNA中的O8G修饰,并通过分析cDNA中O8G > T突变在单核苷酸分辨率上确定O8G位置。
RNA中的O8G会导致异常质量和蛋白翻译的保真度问题,从而受到RNA衰减途径的影响。除氧化损伤外,8-oxo-dG也是一种表观遗传修饰,可影响转录调控元件和其他表观遗传修饰。
为了系统性揭示RNAO8G氧化修饰,云序生物提供了成熟的RNA O8G氧化修饰测序服务。技术原理如下:将RNA O8G氧化特异性抗体与被随机打断的RN**段进行共孵育,抓取有O8G氧化修饰的片段进行测序;同时需要平行测序一个对照(Input)样本,对照样本为未进行IP反应的RN**段。对照样本用于消除非特异性抓取O8G氧化片段的背景。对比免疫共沉淀IP样本和Input样本中的序列片段,将O8G氧化修饰位点定位到转录组上,并根据RNA-seq数据,计算样本中O8G氧化程度。
配合专业的生物信息学分析,云序生物可进一步提供高精度的O8G氧化图谱,帮助客户揭示O8G氧化在生物学功能和潜在的作用机制。
云序特色
*全产品线:可针对性地检测不同类型RNA分子的O8G氧化;
特异性高:特异性富集和检测O8G氧化的 RN**段;
全转录组覆盖:全转录组范围的RNAO8G氧化检测;
全物种检测:可以检测几乎任何动植物的O8G氧化;
专业化的生信分析:强大的生信团队,专业的O8G氧化数据分析;
产品分类
O8G全转录组测序:同时检测O8G氧化的环状RNA,LncRNA和mRNA;
O8G 环状RNA测序:检测O8G氧化的所有环状RNA;
O8G LnRNA测序:同时检测O8G氧化的LncRNA和mRNA;
O8G mRNA测序:检测O8G氧化的所有mRNA;
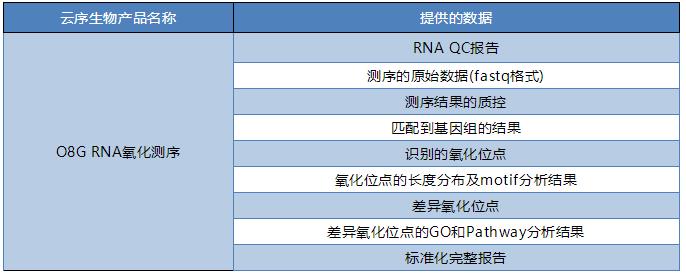
数据分析
优势二:累计完成数千例 RNA甲基化测序样本,覆盖医口、农口等各类样本。
优势三:可检测mRNA和各类非编码RNA(circRNA,lncRNA,Pri-miRNA等)。
优势四:提供O8G-seq、MeRIP-qPCR验证、RIP和RNA pull-down等。
优势五:超微量MeRIP测序,RNA量低至500ng起。
相关产品
往期回顾
客户文章|1区,m5C RNA甲基化测序&5mC DNA甲基化测序助力番茄果实成熟机制研究
客户文章|m6A甲基化测序助力脓毒症诱导的ARDS表位机制研究

